DIASORIN: ANALISI FONDAMENTALE
Diasorin [DIAS.MI], società attiva nei test diagnostici, ha annunciato i seguenti dati.
PRINCIPALI RISULTATI DEL 1° SEMESTRE 2020
Fatturato 382,3 milioni, pari a +9,1% (+8,7% a cambi costanti) rispetto a quanto registrato nello stesso periodo del 2019. Ricavi in crescita anche a seguito del contributo dei test di diagnostica molecolare e di immunodiagnostica per il SARS-CoV-2, generati per oltre l'85% nelle Americhe (in particolare negli Stati Uniti) e in alcuni paesi europei. Da segnalare l'aggiudicazione di alcuni importanti contratti governativi in Canada, Regno Unito, Belgio ed Israele per condurre studi epidemiologici sulle rispettive popolazioni. L'andamento del business ex-COVID ha registrato un calo pari a -17,3%a cambi costanti.
Ebitda: 153,6 milioni, +10,3% (+10,1% a cambi costanti) rispetto allo stesso periodo del 2019, pari al 40,2% del fatturato. Il risultato è conseguenza della crescita delle vendite e della leva operativa che ha consentito di ridurre l'incidenza delle spese sui ricavi.
Ebit: 123,6 milioni, +12,2%. Incidenza sul fatturato: 32,3%.
Utile netto: 94,7 milioni, +12,8%. Incidenza sul fatturato: 24,8%.
Posizione finanziaria netta: +190,4 milioni al 30 giugno 2020 (+172,9 milioni al 31 dicembre 2019). La variazione, pari a +17,5 milioni, include la distribuzione dei dividendi, pari a 52,0 milioni, deliberati dall'Assemblea degli Azionisti in data 10 giugno 2020.
Free cash flow: 73,9 milioni nel 1° semestre 2020 (69,5 nel 1° semestre 2019).
INSTALLAZIONE ANALIZZATORI IMMUNODIAGNOSTICA:
saldo netto nel 1° semestre 2020pari a+241 unità, per un totale di 8.530 unità al 30 giugno 2020. Si segnala l'ottimo andamento delle installazioni del LIAISONXL, pari a complessive +282 unità.
GUIDANCE:
tenuto conto dell'attuale stato di incertezza ed imprevedibilità del contesto macroeconomico post COVID-19 a livello mondiale, DiaSorin ritiene opportuno confermare la scelta operata in occasione della pubblicazione dei risultati del 1° trimestre e pertanto non fornire ancora previsioni in merito all'evoluzione della gestione per l'esercizio 2020.
Nonostante ciò, a seguito della buona performance del business nel 1° semestre e in considerazione del settore in cui DiaSorin opera, il management non si aspetta ripercussioni negative sui risultati del Gruppo nel 2° semestre dell'esercizio e si riserva di dare un aggiornamento al Mercato qualora si abbia una maggiore visibilità sulla prevedibile evoluzione del business.
BUSINESS DEVELOPMENT:
Firma di un accordo di licenza esclusiva e di trasferimento di tecnologia con TTP plc, in base al quale DiaSorin avrà accesso alla piattaforma PuckdxTM che consente l'automazione dell'analisi diagnostica sul campione clinico; l'accordo è in linea con la strategia di Gruppo di rendere disponibili i test di diagnostica molecolare su una piattaforma Point-of-Care.
SVILUPPO TEST DI IMMUNODIAGNOSTICA:
lancio di due test sierologici in risposta alla pandemia da COVID-19:LIAISON®SARS-CoV-2S1/S2 IgG e LIAISON®SARS-CoV-2IgM.
Entrambi i test hanno marcatura CE e sono stati approvati dalla Food and Drug Administration (FDA) statunitense con l'autorizzazione all'uso per emergenza sul mercato locale (EUA). Il test LIAISON® SARS- CoV-2 S1/S2 IgG, inoltre, ha ottenuto l'approvazione alla commercializzazione nei mercati brasiliano e canadese ed è stato adottato da 4 governi (Israele, Belgio, Canada e Regno Unito), per condurre studi epidemiologici sulle rispettive popolazioni.
SVILUPPO TEST DI DIAGNOSTICA MOLECOLARE:
lancio di due test in risposta alla pandemia da COVID-19:SimplexaTMCOVID-19Direct Kit e SimplexaTMFlu A/B & RSV Direct Gen II Assay.
Il primo, marcato CE e con l'autorizzazione all'uso per emergenza sul mercato statunitense (EUA), individua la presenza del SARS-CoV-2 da tampone rinofaringeo. Il secondo, marcato CE, identifica i ceppi influenzali di tipo A e B ed il virus respiratorio sinciziale (RSV), consentendo la diagnosi differenziale tra queste infezioni e quella da SARS-CoV-2 quando eseguito in contemporanea al SimplexaTM COVID-19 Direct Kit.
lancio del test, marcato CE, Simplexa TM Congenital CMV Direct Assay, il primo e unico sul mercato a consentire la rilevazione di DNA del Citomegalovirus direttamente su campioni di saliva e urina di neonati fino al ventunesimo giorno dalla nascita.
Raccomandazione POCO INTERESSANTE con un prezzo obiettivo a 147 euro.
La società è in prima linea contro il Covid-19 e si gioca alcune carte importanti nel segmento della diagnostica, ma siamo convinti che ai prezzi attuali il titolo sconti già ampiamente il potenziale di miglioramento.
Peraltro, persiste una certa incertezza sull'evoluzione del quadro futuro. A livello di guidance, la società, “tenuto conto dell’attuale stato di incertezza ed imprevedibilità del contesto macro-economico post COVID-19 a livello mondiale, ritiene opportuno ... non fornire ancora previsioni in merito all’evoluzione della gestione per l’esercizio 2020. Nonostante ciò, a seguito della buona performance del business nel 1° semestre e in considerazione del settore in cui DiaSorin opera, il management non si aspetta ripercussioni negative sui risultati del Gruppo nel 2° semestre”.
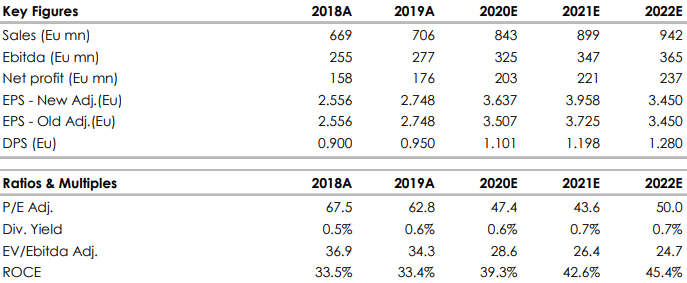
Nella tabella i dati storici (A) e prospettici (E) elaborati da Websim/Intermonte.
www.websim.it
Azioni menzionate
Advertisment