DIASORIN: ANALISI FONDAMENTALE
Diasorin [DIAS.MI], società attiva nei test diagnostici, ha annunciato che il suo test sierologico IgG è stato scelto dal sistema sanitario UK per uno screening su base nazionale con lo scopo di tracciare l’impatto e la diffusione del coronavirus tra la popolazione.
Il Regno Unito è il quarto Paese ad aver scelto il test sierologico di Diasorin.
La notizia conferma l’elevata qualità dei test di Diasorin, ma non è stata fornita alcuna indicazione su due fattori determinanti: volumi e prezzi. Le nostre stime sull’anno già includono un supporto complessivo di circa 60 milioni di euro dalla vendita dei test sierologici a valle delle indicazioni fornite del management sulla possibilità di raddoppiare la capacità produttiva (da 5 milioni/mese a 10 milioni/mese).
Pochi giorni prima Diasorin ha annunciato il test Simplexa™ Flu A/B & RSV Direct Gen II con marcatura CE, progettato per la piattaforma LIAISON® MDX e lo ha sottoposto anche alla FDA per la validazione negli USA.
Il test molecolare è in grado di identificare i ceppi influenzali di tipo A e B ed il virus respiratorio sinciziale (RSV) in modo diretto (senza estrazione degli acidi nucleici) e offre flessibilità nella gestione delle diagnosi e può essere eseguito separatamente o contemporaneamente al test Simplexa COVID-19 Direct, permettendo una diagnosi che differenzi l’infezione da SARS-CoV-2, da influenza di tipo A o B e da RSV. Ad oggi, sono state validate con il test Simplexa più di 100 varianti di influenza, incluse quelle del vaccino anti-influenzale 2020/2021.
Il test dovrebbe consentire un’analisi differenziale efficace in vista della prossima stagione influenzale, considerando anche le possibili complicazioni legate dalla circolazione del SARS-COV2 nella popolazione. Al momento è prematuro stimare l’upside sul fatturato (che riteniamo ragionevolmente contenuto), ma la possibilità di effettuare il test contemporaneamente a quello molecolare per il Covid-19 (upside di ca. Eu12mn/mese secondo le indicazioni del management) potrebbe garantire un buon supporto almeno per tutta la durata della stagione influenzale nel prossimo autunno inverno.
Diasorin ha presentato i seguenti dati del primo trimestre 2020
Il primo trimestre 2020 è terminato con un utile netto in calo a 37,7 milioni (-6,6% rispetto allo stesso periodo dell'anno scorso).
Il fatturato sale a 174,6 milioni (+2,3%) e registra una crescita nonostante la contrazione dei volumi di test di routine nelle geografie più colpite dal Covid-19, in particolare Cina, Italia e Stati Uniti.
Le vendite di diagnostica molecolare sono positive nel trimestre (+47,9% a tassi di cambio costanti) 'anche grazie al lancio in Europa e
Stati Uniti a fine marzo del test per la diagnosi rapida del Covid-19 e all'aumento del fatturato del test per l'influenza soprattutto nel mercato americano'.
Diasorin ha lanciato nel mese di marzo un test molecolare su piattaforma proprietaria LIAISON MDX, che a partire dal tampone
consente l'individuazione del virus entro 1,5 ore contro le 6-8 ore dei sistemi concorrenti. A seguire, nel mese di aprile, è stato sviluppato e commercializzato su piattaforma LIAISON XL un test sierologico per ricercare la presenza degli anticorpiIgG neutralizzanti in risposta all'infezione. Entrambi i test hanno marcatura CE ed hanno ottenuto l'autorizzazione ad uso di emergenza da parte della Food and Drug Administration.
L'Ebitda è in calo a 64,5 milioni (-4,5%).
Nel corso del trimestre è stato registrato un costo 'one-off' pari a 3,3 milioni nella filiale sudafricana. Al netto di questa voce straordinaria,
l'Ebitda sarebbe stato pari a 67,8 milioni.
La posizione finanziariaa netta è pari a +215,5 milioni a fine marzo 2020, in incremento di 42,6 milioni rispetto al termine del 2019.
Diasorin ha deciso di ritirare la propria guidance 2020, riservandosi di dare un aggiornamento non appena si avrà maggiore visibilità sulla prevedibile evoluzione del business a seguito della pandemia.
News post trimestrale.
Diasorin ha ricevuto il via libera dalle autorità canadesi per la vendita del test sierologico che ricerca la presenza degli anticorpi IgG neutralizzanti in risposta all’infezione da Covid-19, che segue l'ok da parte della Food and Drug Administration statunitense, mentre in Italia la società con base a Saluggia nel Vercellese non fornirà i test per il governo. E' quanto ha detto il Ceo del gruppo specializzato nella diagnostica, Carlo Rosa, in una call con gli analisti sui risultati del primo trimestre.
"Sui test sierologici i governi di altri Paesi, come Belgio e Israele, stanno rispondendo bene e la scorsa notte abbiamo avuto il via libera da parte del Canada per il test sierologico e di questo siamo molto orgogliosi. Per quanto riguarda l'Italia il governo ha deciso di prendere un'altra strada e di affidare ad Abbott test sierologici su 150.000 persone. Ci sono molti Paesi dove andremo a fornire questo test, ma non al nostro governo", ha sottolineato Rosa.
Il manager ha poi aggiunto che l'azienda punterà a incrementare la capacità produttiva di questi test per fare fronte alla crescente domanda, portandoli da 5 a 10 milioni di test al mese.
Infine, per quanto riguarda il test molecolare su piattaforma proprietaria LIAISON MDX, che a partire dal tampone consente l’individuazione del virus entro 1,5 ore contro le 6-8 ore dei sistemi concorrenti, Rosa ha rivisto al rialzo le stime di ricavi incrementali "dai precedenti 5-10 milioni a 10-12 milioni al mese. Ci attendiamo che la capacità salga un po' e che continui a svilupparsi su base mensile".
Diasorin ha fornito a oggi 150.000 test sierologici alla Regione Lombardia.
L'azienda lodigiana Technogenetics ha contestato questo affidamento diretto, comunicando di aver fatto ricorso al Tar, presso il quale si è svolta oggi la camera di consiglio su una richiesta di sospensiva. La decisione è prevista domani.
Le procure di Milano e Pavia, secondo quanto riferito da fonti giudiziarie, hanno aperto due fascicoli di indagine "conoscitive", cioè senza indagati né ipotesi di reato, proprio sull'affidamento diretto con cui la Regione ha incaricato Diasorin dello sviluppo del progetto con l'Ospedale San Matteo di Pavia.
Raccomandazione POCO INTERESSANTE con un prezzo obiettivo a 147 euro.
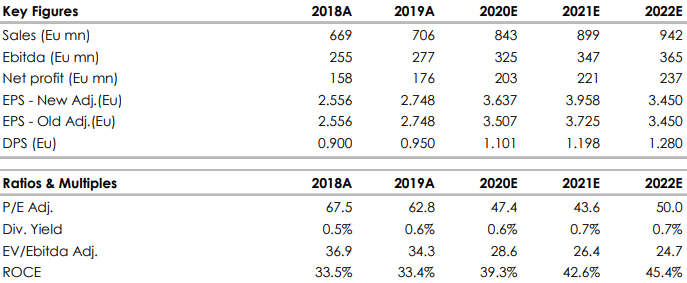
La società è in prima linea contro il Covid-19 e si gioca alcune carte importanti nel segmento della diagnostica, ma siamo convinti che ai prezzi attuali il titolo sconti già ampiamente il potenziale di miglioramento con un multiplo di circa 28,6 volte il margine lordo Ebitda..
Nella tabella i dati storici (A) e prospettici (E) elaborati da Websim/Intermonte.
www.websim.it
Azioni menzionate
Advertisment